RDDC邀您关注血友病:一种需要被看见的隐性遗传病
疾病概述
血友病(Hemophilia)是一种X染色体连锁的隐性遗传性出血性疾病,主要由凝血因子Ⅷ(FⅧ,由F8基因编码)或凝血因子Ⅸ(FⅨ,由F9基因编码)的缺乏或功能异常引起[1]。患者常表现为关节、肌肉和深部组织出血,也可表现为胃肠道、中枢神经系统等内部脏器出血等。若反复出血,不及时治疗可导致关节畸形和(或)假肿瘤形成,严重者可危及生命。外伤或手术后延迟性出血是本病的特点[2]。根据患者缺乏凝血因子的类型,可以分为血友病A(Hemophilia A, HEMA)(FⅧ缺乏)及血友病B(Hemophilia B, HEMB)(FⅨ缺乏)两种类型[3]。
据《中国血友病诊治报告2023》显示,我国血友病患病率在(2.73-3.09)/10万,其中男性患者占据主要比例,女性血友病患者极其罕见。在男性患者中,血友病A的发病率约为1/5000,血友病B的发病率约为1/25000。所有血友病患者中,血友病A占80%~85%,血友病B占15%~20%。血友病的发病率没有种族或地区差异,但由于经济等方面的原因,血友病的患病率在不同国家甚至同一国家的不同时期都存在很大的差异。
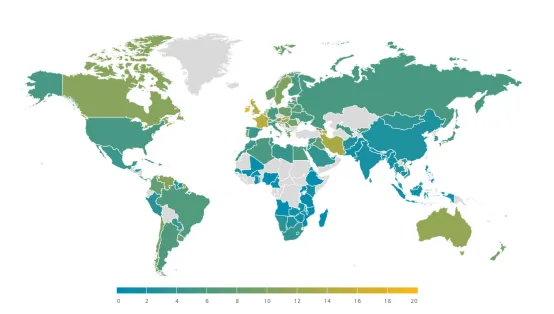
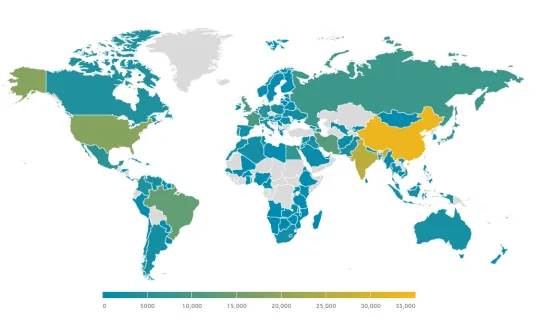
根据WFH(世界血友病联盟)2022年的统计数据(图1&图2),全球范围内,中国血友病的患病率相对较低。然而,考虑到我国庞大的人口基数,实际上患有血友病的人数高达32638人,这使得中国成为全球拥有最多血友病患者的国家。值得注意的是,由于血友病属于罕见病,部分患者可能未能得到正式诊断或记录在案。因此,实际的患者数量可能会高于官方统计的数字。这进一步强调了了解血友病发病机制的重要性,以及为血友病患者及其家属提供更多帮助的紧迫性。
图1. 2022年血友病每10万人患病率
来源:世界血友病联盟(WFH)
图2. 2022年血友病患者全球分布概况
来源:世界血友病联盟(WFH)
致病基因
图3. 近年来血友病发生与基因突变相关性
来源:儿科血友病管理网络(PedNet)
根据儿科血友病管理网络(PedNet)提供的数据(图3),我们得知在血友病患者中,86%的病例源于基因突变。这一数据揭示了血友病的分子基础,并突显了遗传学在理解与治疗该疾病中的核心地位。通过深入研究血友病的遗传学机制,我们可以更好地预测疾病的发生风险,制定预防策略,并为患者提供更有效的治疗方法。
F8基因与血友病A:
⭐️位置:F8基因位于X染色体长臂末端Xq28,包含26个外显子和25个内含子,这些区域在基因表达中起着关键作用。
⭐️功能:F8基因的主要功能是编码凝血因子VIII,这是一种关键的蛋白质,参与血液凝固过程。凝血因子VIII在血液凝固级联反应中发挥重要作用,帮助防止过度出血。
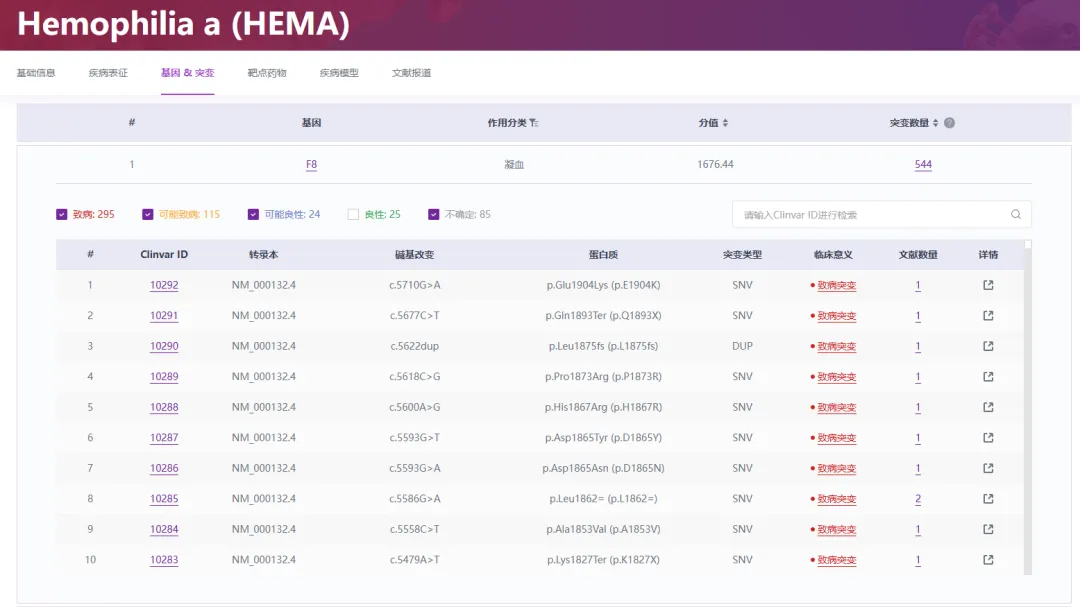
⭐️与血友病A的关系:血友病A是一种遗传性疾病,主要影响男性,因为F8基因位于X染色体上。罕见病数据中心(简称“RDDC”,网址:https://rddc.tsinghua-gd.org/)收录了血友病A与F8基因突变的关系(图4)。数据显示,F8基因有544种突变可能导致或影响血友病A的发生。这些突变包括内含子22倒位、点突变、缺失或异常基因插入等[5,6]。这些突变会导致凝血因子VIII的合成障碍或功能异常,进而引发血友病A。
图4. 血友病A与F8基因突变密切相关
来源:RDDC数据库
F9基因与血友病B:
⭐️位置:F9基因位于X染色体长臂Xq26.3~27.2,包含8个外显子、7个内含子及侧翼序列。
⭐️功能:F9基因为凝血因子IX提供指令,凝血因子IX同样在血液凝固过程中发挥重要作用。
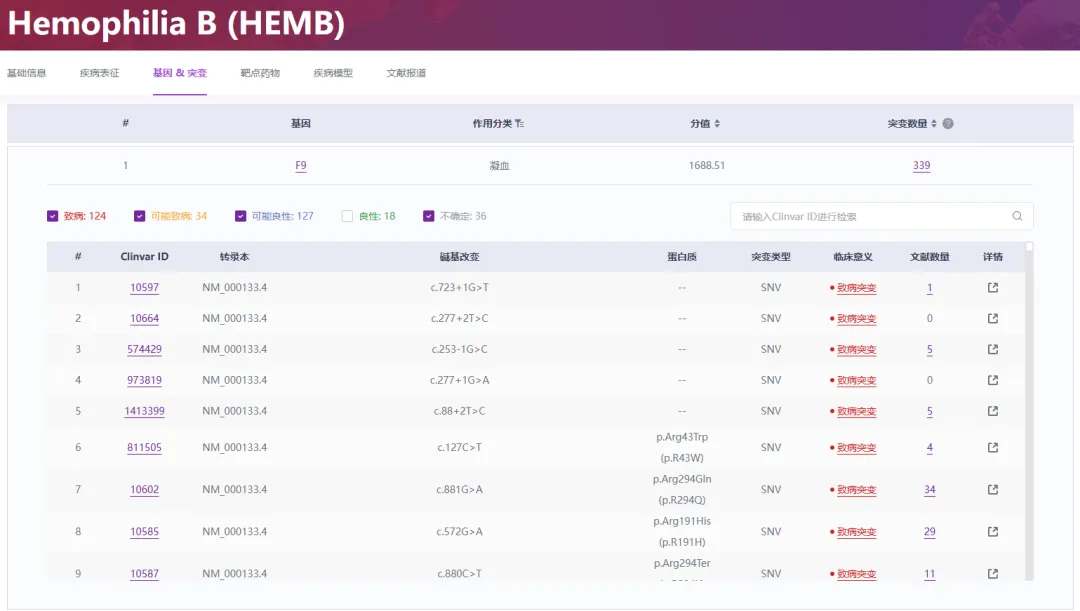
⭐️与血友病B的关系:根据RDDC数据库的记录,血友病B与F9基因的突变有着密切的关系(图5)。目前已知,F9基因有339种不同的突变形式可能会导致或增加血友病B的风险。这些突变类型包括缺失、插入和点突变等[7,8]。当F9基因发生突变时,可能会导致凝血因子IX的合成减少或其功能出现异常,从而引发血友病B。
图5. 血友病B与F9基因突变密切相关
来源:RDDC数据库
了解更多血友病基因信息,欢迎登陆RDDC官网,即可免费查阅!
动物模型
鉴于人类与大鼠和小鼠基因的高度相似性,这两种啮齿类动物在血友病的遗传学和治疗研究中扮演着关键角色。它们的基因组结构与人类相近,因此成为理解血友病遗传机制、测试新疗法及开发治疗策略的重要模型。
选择大鼠和小鼠作为研究模型具有多重优势:它们繁殖迅速,成本较低,且其生物学特性和生理反应近似于人类。这使得科研人员能在控制条件下进行实验,以探究血友病的遗传原因、病理发展过程,以及评估新治疗方法的效果。
当前生物医学实验中常见的血友病模型小鼠主要包括:
1. 血友病A小鼠模型(F8缺陷):这种模型的F8基因被敲除或突变,导致无法正常合成F8,表现出严重的出血倾向,如关节出血、皮肤出血、鼻出血等,并可能伴有生长发育迟缓、贫血等症状。
2. 血友病B小鼠模型(F9缺陷):在此模型中,F9基因被敲除或突变,导致无法正常合成F9,同样表现出严重的出血倾向及其他相关症状。
3. 重组凝血因子治疗模型:通过导入人类凝血因子F8或F9基因,使小鼠能正常合成凝血因子,模拟血友病患者的病情。这些小鼠在接受治疗后,出血倾向明显改善,但需要定期注射以维持效果。
4. 基因编辑模型:利用CRISPR/Cas9等技术精确编辑小鼠的F8或F9基因,模拟血友病患者的遗传变异。这些小鼠展现出与患者相似的出血倾向和症状,并可用于研究基因编辑技术在血友病治疗中的应用。
治疗前景——基因治疗
血友病的治疗领域正迎来显著的突破与革新。过去,我们主要依赖于注射血浆或输注凝血因子的传统替代疗法,这些疗法既有应急式的按需治疗,也有规律性的预防性治疗[9]。然而,随着生命科学技术的飞速进步,基因治疗已经崭露头角,正逐渐成为单基因疾病治疗的新潮流。
近三十年来,血友病A(HA)和血友病B(HB)在基因治疗领域尤为突出,成为了推动该领域发展的模型疾病[10]。基因治疗为血友病患者带来了全新的治疗可能性,因为它能够实现凝血因子的持续内源性表达。这一创新的治疗方式不仅有效消除了突破性出血和微出血的风险,还显著减少了因合并症和频繁医疗干预而给患者带来的负担。更为重要的是,它极大地提高了患者的生活质量,为血友病患者带来了前所未有的治疗希望[11]。
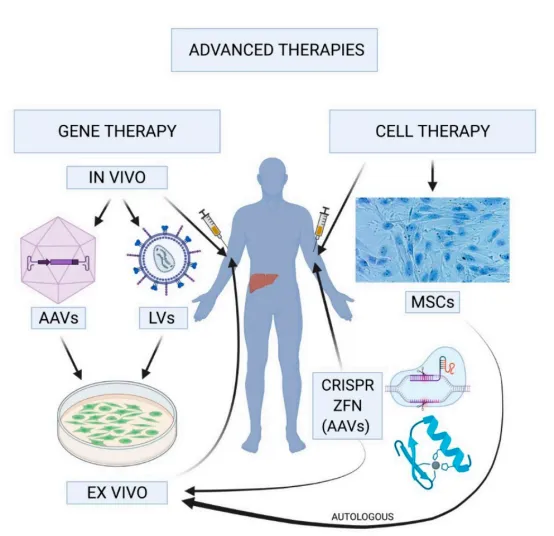
图6. 血友病基因治疗工作原理[12]
图6展示了血友病的基因治疗策略,主要分为体内基因治疗和体外基因治疗两大类:体内基因治疗涉及将含有“治疗基因”的载体,例如腺相关病毒(AAV)或慢病毒(LV),通过全身性的注射方式输送到患者体内。这种方法直接在患者体内实施,旨在通过引入功能性基因来纠正遗传缺陷,从而治疗疾病。相比之下,体外基因治疗则首先需要在体外环境中对自体或同种异体细胞进行转染操作,这些经过基因修饰的细胞在培养基中扩增后,再被输回至患者体内。此方法的优势在于可以对细胞进行精确的基因编辑,并在控制的环境中验证其安全性和有效性之后,再将其应用于患者。这两种策略都旨在通过基因层面的干预,为血友病患者提供更为精准和持久的治疗效果。通过选择合适的策略,可以为患者提供个性化的治疗方案,以达到最佳的治疗效果。
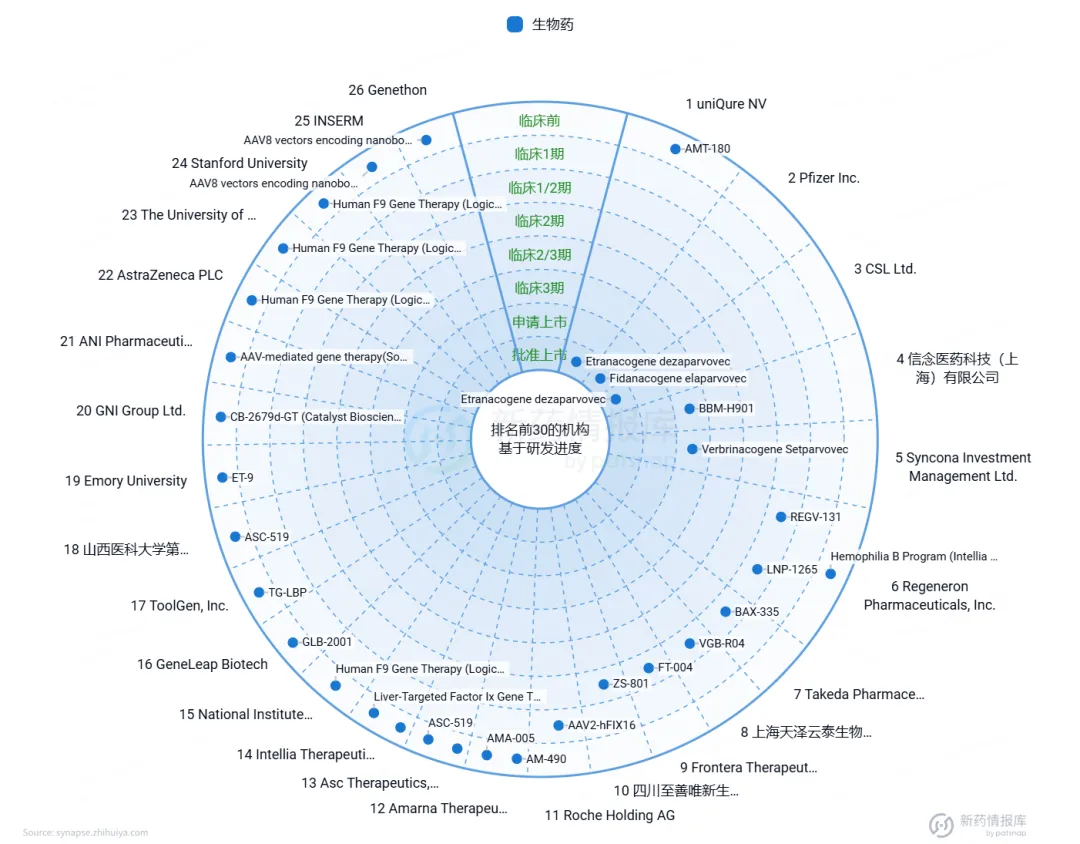
根据智慧芽新药情报库上的统计资料,血友病A和血友病B的基因治疗药物研发领域正经历着显著的发展。在医学科技不断进步的今天,针对血友病B的F9基因,已有Etranacogene dezaparvovec和Fidanacogene elaparvovec药物获批上市(图7)。
图7. 血友病B的基因治疗药物研发现状
来源:智慧芽新药情报库
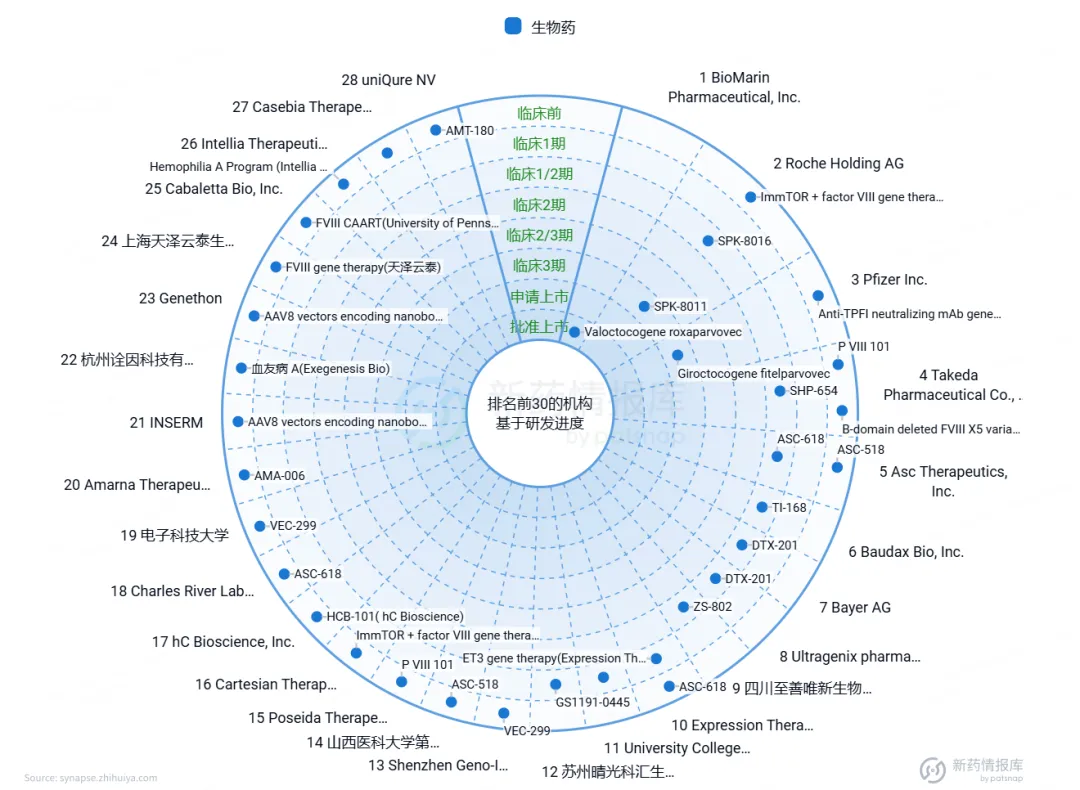
针对血友病A的基因治疗药物:Valoctocogene roxaparvovec已获批上市,虽然这个药物的靶向基因为F10(图8)。这些进展不仅标志着科研工作者不懈的努力,也给患者带来了新的希望。
图8. 血友病A的基因治疗药物研发现状
来源:智慧芽新药情报库
此外,还有近60种基因治疗药物正处于临床或临床前试验阶段。这些潜在疗法的研发背后,是来自全球各地制药企业的共同努力。其中,Pfizer、BioMarin等全球知名的制药企业赫然在列,他们凭借雄厚的科研实力,为血友病的治疗贡献了重要的力量。同样值得注意的是,多家中国药企也在积极参与其中,如信念医药科技(上海)有限公司、苏州诺洁贝生物技术有限公司、苏州晴光科汇生物科技有限公司等。他们的参与不仅展现了国内外制药行业对于血友病基因治疗药物开发的高度重视,也体现了中国在全球医药研发领域的活跃参与和贡献。
这些成果不仅是科技进步的体现,更是对广大血友病患者的希望之光。随着更多的基因治疗药物进入临床试验阶段,未来有望为血友病患者提供更多、更有效的治疗选择。同时,这也预示着血友病治疗领域的研发方向正在从传统的蛋白替代疗法转向更为前沿的基因治疗技术,为全球医药研发领域的创新和发展注入新的活力。
RDDC助力罕见病研究
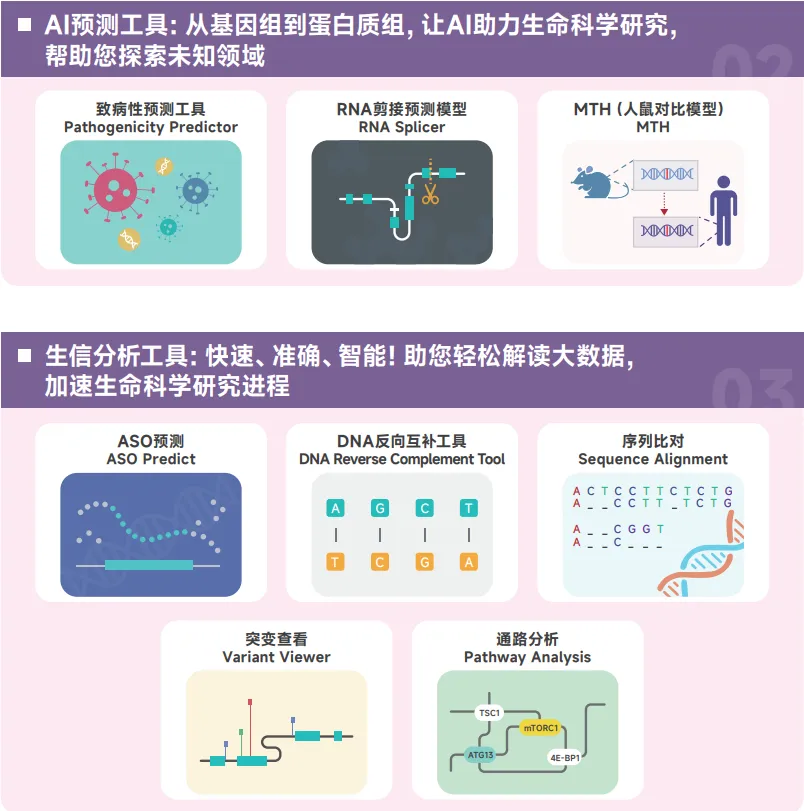
罕见病数据中心(Rare Disease Data Center,简称“RDDC”),是由联盟内成员单位合作开发的关于罕见病研究的数据库。RDDC整合了全球开源的流行病学、药物研发、疾病相关基因图谱、基因突变位点、大小鼠实验动物模型等数据信息,再结合人工智能、生物信息等先进技术,部署了致病性预测工具(Pathogenicity Predictor)、RNA剪接预测模型(RNA Splicer)、通路分析(Pathway Analysis)等一系列AI、生信工具,赋能罕见病诊疗研究工作。
欢迎感兴趣的用户复制链接(https://rddc.tsinghua-gd.org)体验RDDC网站。
声明:本文收集归纳的信息,如有错漏,欢迎批评指正!
参考资料:
[1]E. Berntorp, K. Fischer, D.P. Hart, M.E. Mancuso, D. Stephensen, A.D. Shapiro, V. Blanchette, Haemophilia, Nat Rev Dis Primers 7(1) (2021) 45.[2]国家卫生健康委罕见病诊疗与保障专家委员会办公室, 罕见病诊疗指南(2019 年版), (2019) 214-220.
[3]P.H. Bolton-Maggs, K.J. Pasi, Haemophilias A and B, Lancet 361(9371) (2003) 1801-9.
[4]Consensus of Chinese expert on the diagnosis and treatment of hemophilia (version 2017), Zhonghua Xue Ye Xue Za Zhi 38(5) (2017) 364-370.
[5]Y. Liu, D. Li, D. Yu, Q. Liang, G. Chen, F. Li, L. Gao, Z. Li, T. Xie, L. Wu, A. Mao, L. Wu, D. Liang, Comprehensive Analysis of Hemophilia A (CAHEA): Towards Full Characterization of the F8 Gene Variants by Long-Read Sequencing, Thromb Haemost 123(12) (2023) 1151-1164.
[6]T.J.S. Lopes, R. Rios, T. Nogueira, R.F. Mello, Prediction of hemophilia A severity using a small-input machine-learning framework, NPJ Syst Biol Appl 7(1) (2021) 22.
[7]A. Dericquebourg, M. Fretigny, N. Chatron, B. Tardy, C. Zawadzki, H. Chambost, C. Vinciguerra, Y. Jourdy, Whole F9 gene sequencing identified deep intronic variations in genetically unresolved hemophilia B patients, J Thromb Haemost 21(4) (2023) 828-837.
[8]V. Labarque, M.E. Mancuso, M. Kartal-Kaess, R. Ljung, T.S. Mikkelsen, N.G. Andersson, F8/F9 variants in the population-based PedNet Registry cohort compared with locus-specific genetic databases of the European Association for Haemophilia and Allied Disorders and the Centers for Disease Control and Prevention Hemophilia A or Hemophilia B Mutation Project, Res Pract Thromb Haemost 7(1) (2023) 100036.
[9]P.M. Mannucci, Hemophilia therapy: the future has begun, Haematologica 105(3) (2020) 545-553.
[10]B.J. Samelson-Jones, L.A. George, Adeno-Associated Virus Gene Therapy for Hemophilia, Annu Rev Med 74 (2023) 231-247.
[11]A.C. Nathwani, Gene therapy for hemophilia, Hematology Am Soc Hematol Educ Program 2019(1) (2019) 1-8.
[12]E.C. Rodríguez-Merchán, J.A. De Pablo-Moreno, A. Liras, Gene Therapy in Hemophilia: Recent Advances, Int J Mol Sci 22(14) (2021).