新设计的AAV载体,药物递送效率领先AAV9三倍多
近日,来自Pardis Sabeti实验室的研究团队发表了一篇论文《新型AAV衣壳有助于增强猕猴中枢神经系统中的转基因表达》,研究结果显示,新设计的AAV在将药物输送到灵长类动物大脑的能力是AAV9载体的三倍多。
图1.论文发表于MED
研究背景
腺相关病毒(AAV)载体由于其低免疫原性和促进分裂细胞和非分裂细胞中长期基因表达的能力,是中枢神经系统(CNS)基因治疗应用的首选载体。基于重组AAV(rAAV)的天然AAV血清型治疗的临床和临床前研究已经显示出了治疗各种中枢神经系统疾病的希望。然而,由于血脑屏障(BBB)的保护作用和天然AAV血清型广泛的组织趋向性,rAAV在中枢神经系统转导中的作用受到了限制,这共同导致了中枢神经系统中靶细胞群的转导效率低下。
研究方法
在本实验中,在多个小鼠品系中使用了一种基于mRNA的定向进化策略。此外,还在食蟹猕猴中使用从头选择来识别在大脑中具有增强效力的工程载体。Sabeti实验室的研究生Allie Stanton专注于确定穿透血脑屏障的AAV,她所在的研究小组利用Sabeti实验室的一种名为DELIVER的方法,开发出了PAL AAV。新型AAV能够将“货物”递送到灵长类动物大脑的能力是AAV9载体的三倍多。这个称为PAL家族的AAV载体可能是一种更安全、更有效的向大脑提供基因治疗的方法。
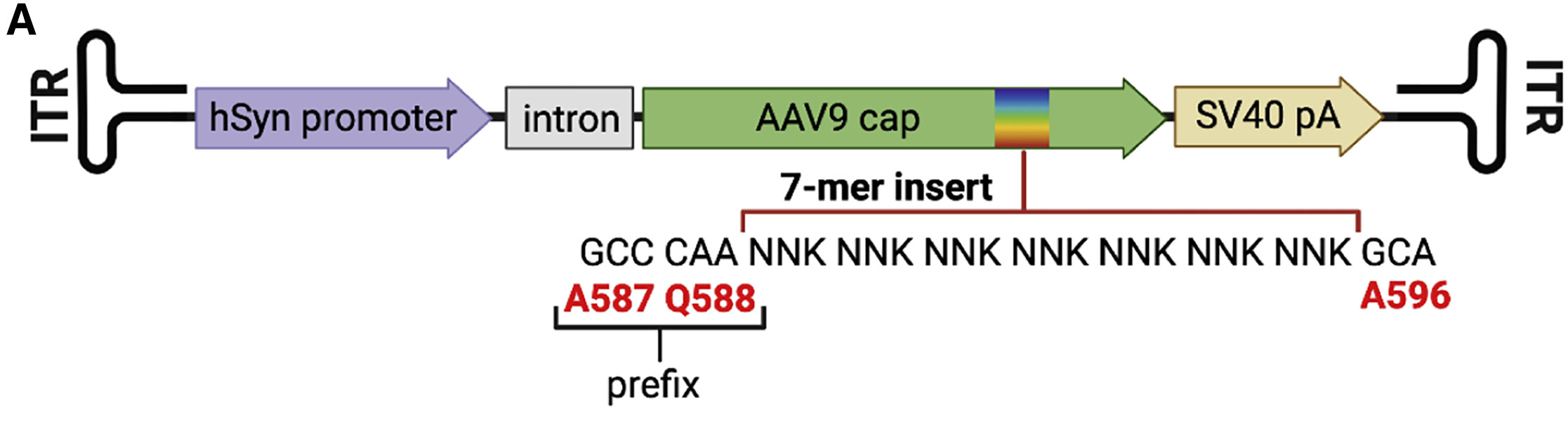
图2.DELIVER的自包装衣壳库构造图
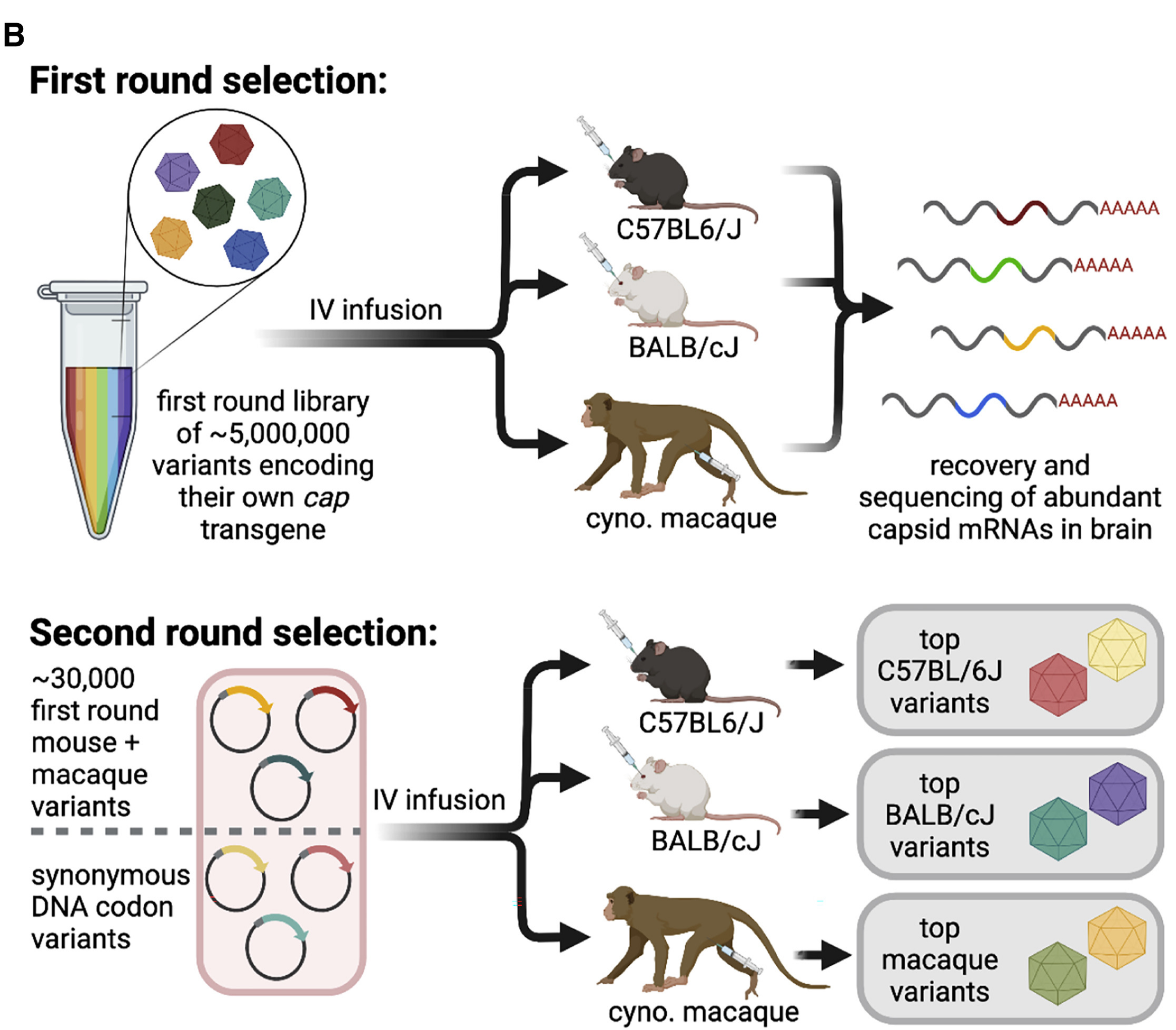
图3.使用DELIVER进行选择的示意图
研究结果
这种新型AAV可以穿过血脑屏障,而血脑屏障通常会阻止许多药物进入大脑。经过工程改造的AAV衣壳在肝脏中的积累也比AAV9少得多,这可能降低了基于AAV9基因疗法的肝脏副作用,这是一种更安全有效的将基因疗法传递到大脑的方式。

图4.实验原理
研究小组还发现,经过改造的病毒对大脑有独特的吸引力。接受PAL治疗的猕猴肝脏中的病毒物质是接受AAV9治疗的灵长类动物的四分之一,这表明新型AAV可以穿过血脑屏障,降低肝脏毒性。
研究结论
本次的实验结果将为更有效的病毒载体提供一个起点。Sabeti表示:“我们对PAL系列AAV的早期结果感到鼓舞,可以看到几个有前途的研究方向,利用定向进化和工程技术改造进一步提高它们的效率。”
补充资料
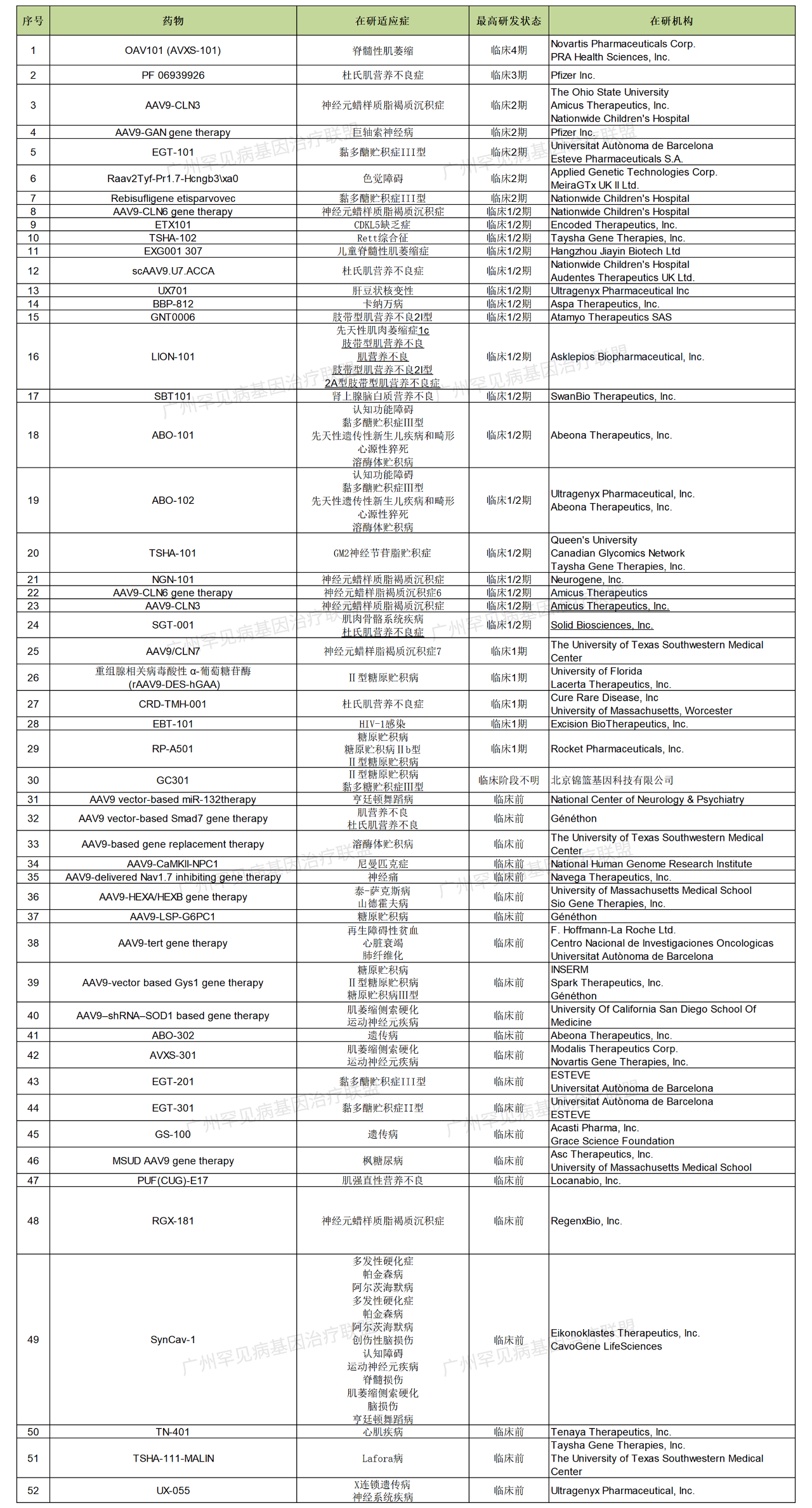
AAV9是一种新近发现的来源于人类的血清型,对心肌细胞具有明显的组织特异性,能够透过血脑屏障,转导神经细胞和脊髓,在治疗神经系统疾病上拥有较大的潜力,成为治疗心脑血管系统疾病理想的载体,因此,小编也搜集整理了目前AAV9的各项研究进展,详情见表1,如有错漏,欢迎批评指正。
表1.AAV9各项研究进展
参考资料:
www.genengnews.com
www.cell.com
synapse.zhihuiya.com/homepage