Nature子刊丨新型AAV变体,可穿越血脑屏障,还可实现重复给药
细胞类型特异性转基因递送技术在脉管系统研究中起到了至关重要的作用。然而,由于选择有限,对于脉管系统的研究受到了很大的阻碍。目前,腺相关病毒(AAV)被认为是一种将基因递送到大脑的有效工具。然而,这种方法需要进行颅内注射给药,可能会导致大脑组织损伤,并且空间覆盖范围有限且不均匀。此外,系统性AAV递送虽然提供了一种无创的方法,但是难以特异性靶向特定细胞类型。
为了克服这些问题,加州理工学院Viviana Gradinaru团队近期开发了一种能够快速穿越血脑屏障,并对大脑细胞具有广泛靶向性的AAV变体,名为AAV-PHP.eB。此外,他们还开发了一种具有细胞类型特异性靶向的AAV变体,名为PHP.V1,它能够穿越血脑屏障,对大脑内皮细胞有更强的靶向作用。然而,这种变体也会靶向星形胶质细胞和神经元,并且需要使用大小受限的启动子,因此其适用范围较为有限。
最近,该团队在Nature Communications上发布了一篇题目为“Functional gene delivery to and across brain vasculature of systemic AAVs with endothelial-specific tropism in rodents and broad tropism in primates”的研究论文。该论文介绍了一种能够靶向特定内皮细胞的系统性AAV递送方法,它可以无创地向全脑递送,同时不会导致大脑组织损伤。这种AAV变体的靶向效果在啮齿动物和灵长类动物中均有广泛应用。该成果为深入研究脉管系统的功能障碍及其对神经系统疾病进展的影响提供了新的工具和方法,也为开发针对这些疾病的治疗方法奠定了基础。
图1.《Nature Communications》官网截图
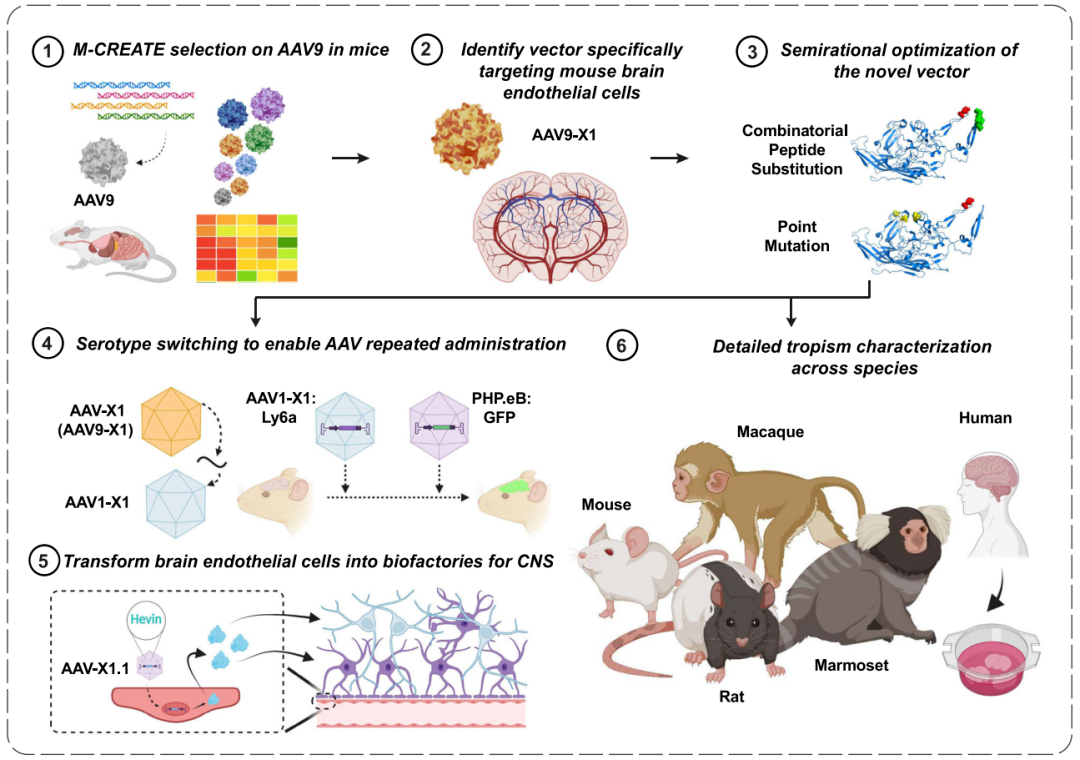
该研究成功设计出一种基于AAV9的新型载体AAV-X1,对啮齿类动物(小鼠、大鼠)进行系统性给药后,能够高效、特异性地转导到大脑内皮细胞,而且在非人灵长类动物(狨猴、恒河猴)和离体人脑切片的中枢神经系统中也能够高效转导。此外,经过衣壳修饰后,AAV-X1的适应血清型范围扩展至AAV1、AAV-DJ等,可实现AAV在基因治疗中的重复给药。
该研究证实了这种脑内皮细胞特异性靶向的AAV可以通过系统性给药穿越血脑屏障,将小鼠脑脉管系统转化为功能性生物工厂,用于中枢神经系统的疾病治疗。作为体内基因治疗递送载体,AAV载体已经被用于治疗多种疾病。本研究所开发的AAV-X1靶向大脑脉管系统,既可以作为中枢神经系统更好的生物工厂,用于表达治疗性蛋白,也为治疗中枢神经系统疾病提供了新的策略。
在该研究中,研究团队通过定向进化和半理性工程设计获得了一个基于AAV的家族,包括AAV-X1和AAV-X1.1。这些A AAV变异体能够在小鼠体内特异性和有效地靶向大脑脉管系统内皮细胞。研究团队还在啮齿类动物模型(小鼠和大鼠)、非人灵长类动物(狨猴和恒河猴)以及离体人脑切片中对这些新型AAV进行了表征,证明它们对啮齿动物的大脑内皮特异性细胞靶向和灵长类动物的广泛中枢神经系统靶向。
该研究还证明AAV-X1是一种在中枢神经系统递送神经活性蛋白中可行的载体。研究团队将小鼠脑内皮细胞转化为生产突触原蛋白Sparcl1/Hevin的“生物工厂”。AAV-X1介导的Sparcl1/Hevin在脑内皮细胞中的表达足以挽救Sparcl1/Hevin敲除小鼠的丘脑皮质突触丧失表型。
该研究还指出,由于第一次给药后诱导产生的中和抗体可能会导致重复给药的AAV被中和,所以AAV基因递送面临重复给药难题。然而,通过衣壳修饰,AAV-X1的适应血清型范围扩展至AAV1、AAV-DJ等,可实现AAV在基因治疗中的重复给药。
图2.来源于生物世界
总的来说,该研究开发了一种创新的AAV系统,可在啮齿类动物中实现脑内皮特异性细胞靶向和在啮齿动物和灵长类动物中实现广泛的中枢神经系统靶向,具有重复给药的潜力。这项研究的成果标志着AAV通过重复给药为基因治疗带来了更多的机会,同时也为针对中枢神经系统疾病的治疗提供了新的载体策略。
文章参考于生物世界