颠覆认知!细胞程序性死亡的机制被揭示,科学家发现细胞自主将细胞膜切块导致细胞裂解
导语:细胞程序性死亡是一种重要的细胞生命活动,可以帮助我们去除受损或无用的细胞,从而保持组织和器官的正常功能。而细胞裂解是一种十分复杂的细胞生命现象,此前一直没有完全理解。这两项新发现将有助于我们更深入地研究细胞死亡的机制,并且为未来开发新的药物和治疗疾病提供新的思路和方向。
最近,《Nature》杂志上发表了两篇研究论文,分别由瑞士巴塞尔大学Sebastian Hiller和洛桑大学Petr Broz、斯图加特大学Kristyna Pluhackova领衔的研究团队[1],以及基因泰克公司Vishva M. Dixit和Nobuhiko Kayagaki领衔的研究团队[2]完成。
Hiller团队和Dixit团队分别在两篇《Nature》论文中报道,揭示了膜蛋白NINJ1如何参与细胞程序性死亡及组织损伤的过程。Hiller团队通过高分辨率成像技术,发现当细胞接收到程序性死亡信号后,NINJ1会在细胞膜表面聚集并形成聚合物,类似拉链的结构,打开细胞膜,导致细胞破裂。另一方面,Dixit团队发现通过单抗阻断NINJ1的聚集,可以抑制细胞膜的破裂,从而保护组织免受损伤。
这两项研究的结果再次证实,在细胞程序性死亡导致的细胞破裂过程中,不是由于渗透压的变化胀破的,而是细胞利用NINJ1自主切割细胞膜,导致细胞解体。这一发现具有重大意义,因为癌症细胞对于死亡具有抗性,而神经退行性疾病等疾病则常常是由于细胞死亡导致的。因此,这一发现有望为治疗这些疾病带来革命性的变化。
图1.Hiller团队论文首页截图(图源:奇点网)
基因泰克公司的Dixit和Kayagaki领衔的团队,于2021年1月20日在《Nature》杂志上发表了一项重要的研究成果[3]。为了寻找细胞膜破裂的机制,他们进行了大规模的遗传学筛选,并最终找到了一个名为NINJ1的双重跨膜蛋白,大小约16kDa。研究结果显示,只要删除编码NINJ1的基因,巨噬细胞对焦亡、坏死和凋亡所导致的细胞裂解的响应会受到损害,并且即使细胞已经死亡,细胞膜裂解也会被抑制,说明在细胞死亡过程中,细胞膜裂解是由细胞本身控制的自主过程。
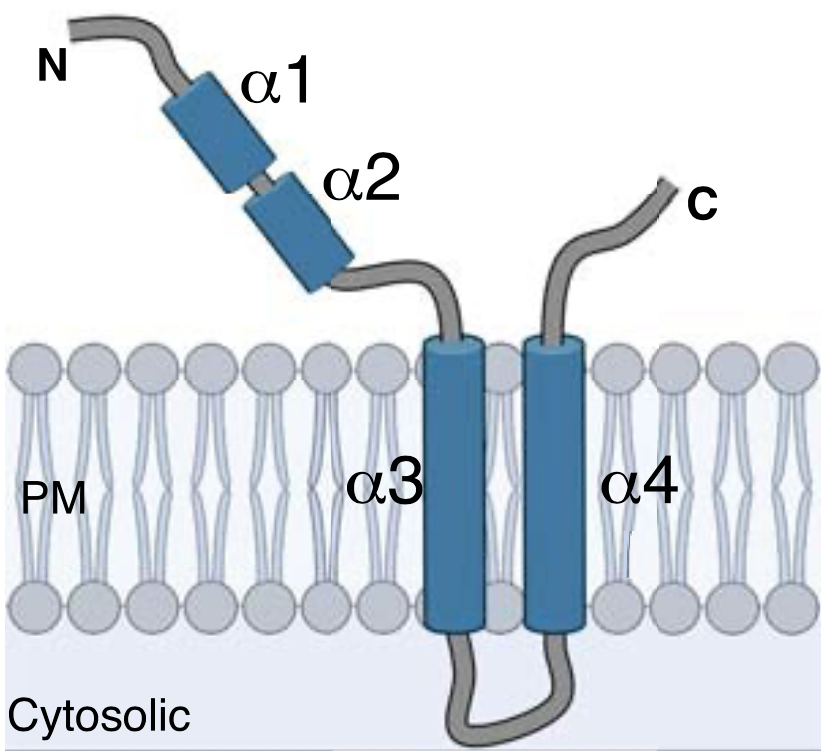
图2.正常情况下,双重跨膜的NINJ1蛋白(图源:奇点网)
这一新的研究成果颠覆了我们一直以来对于细胞死亡相关的细胞膜裂解是被动过程这一普遍认知。然而,在此之前,研究人员对于NINJ1是如何调节细胞膜裂解的,以及NINJ1在介导细胞膜裂解的生理功能方面还存在着缺乏认识的局限。
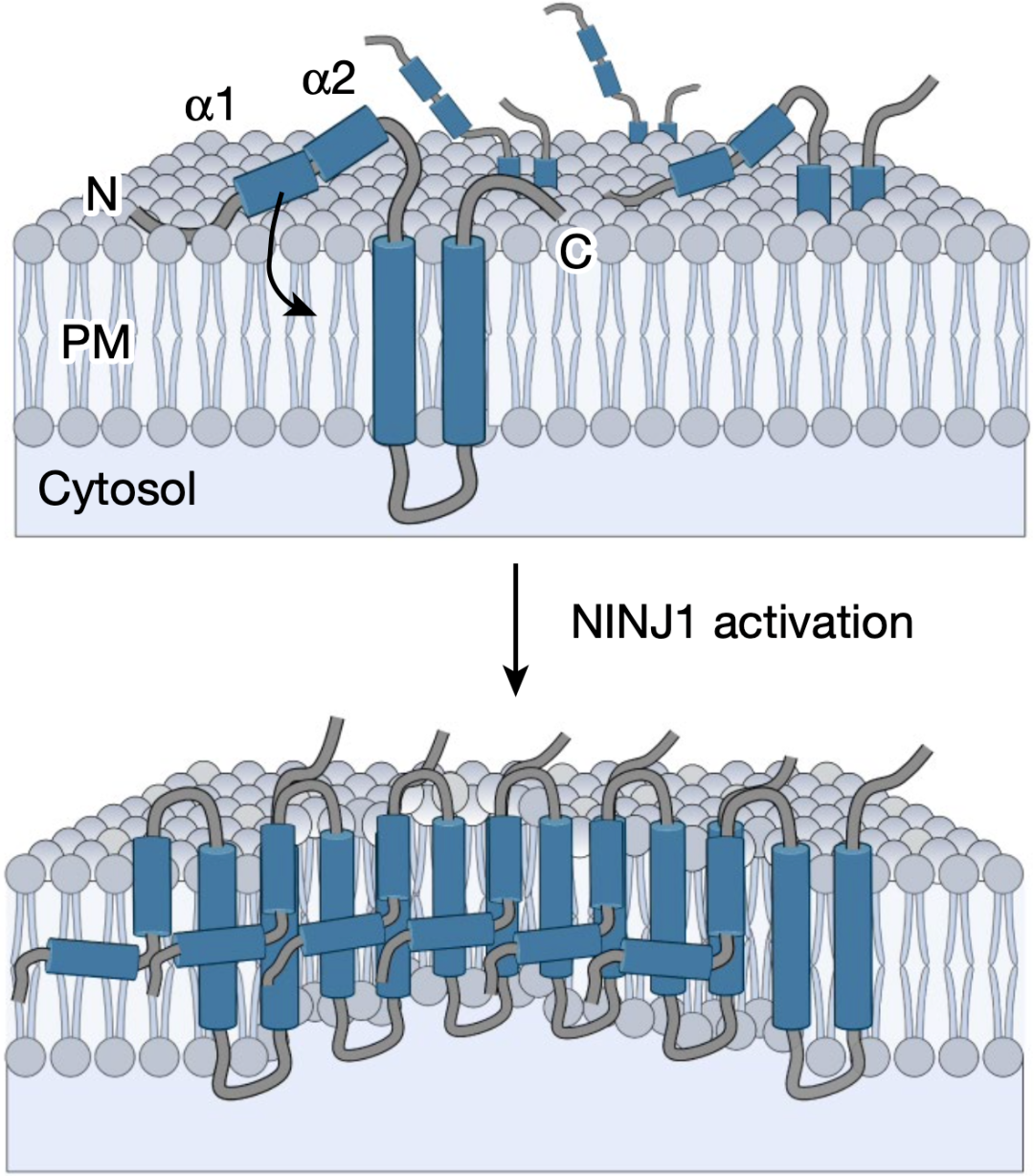
图3.NINJ1的聚集(图源:奇点网)
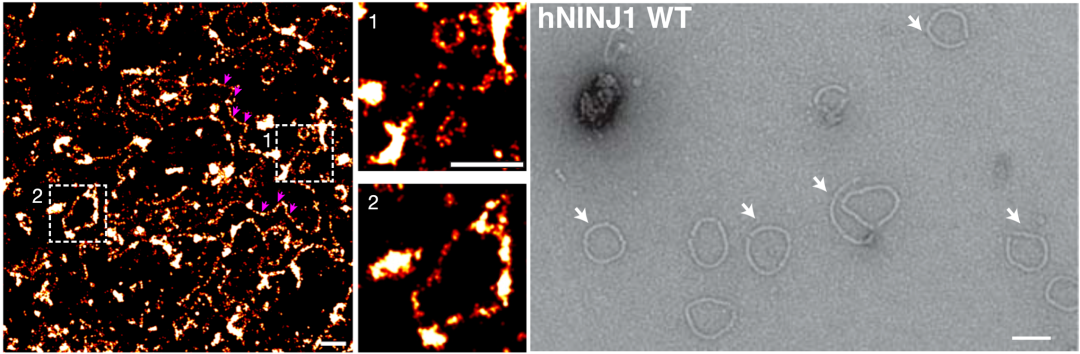
实验结果表明,Hiller团队观察到了长达几微米的NINJ1细丝,其长度约为数百到数千纳米不等。这些NINJ1细丝在巨噬细胞中占比约为10%,包括单丝和双丝,双丝还能形成环状的结构,它们连接着较大的NINJ1聚集体。
图4.超分辨率显微镜下看到的NINJ1聚集体(左图:NINJ1丝,右图:双丝打开后成的环)(图源:奇点网)
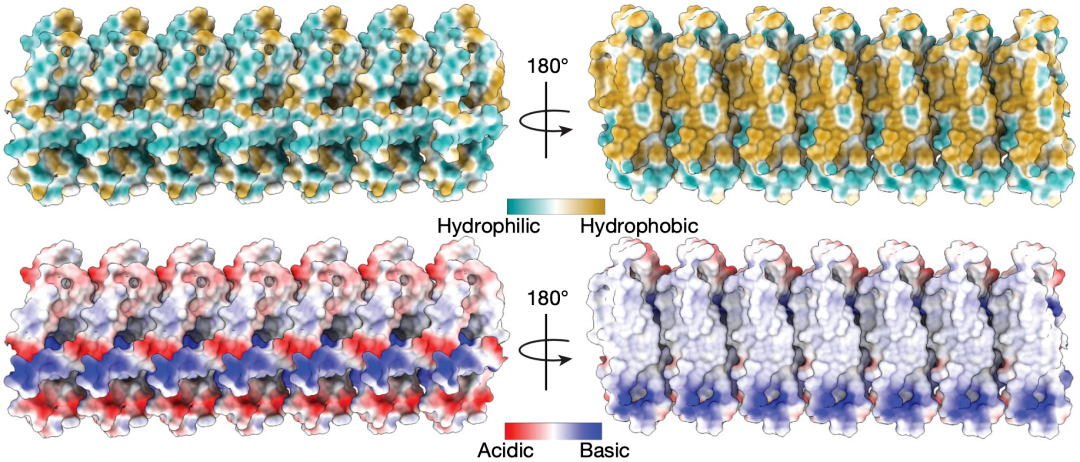
关于NINJ1聚集体如何开启细胞膜,Hiller团队通过研究聚集体的极性得出了答案。他们发现,NINJ1聚集体的两个面极性不同,其中一面是亲水的(由α1和α2螺旋组成),而另一面则是疏水的(有α3和α4螺旋组成),这恰好符合典型成孔蛋白的特点。
图5.NINJ1聚集体极性的分析(图源:奇点网)
在体外实验中,Hiller团队利用45个完整的NINJ1连接在一起,形成了一个完整的圆环,他们发现这个圆环能够持续地维持成一个小孔。
图6.完整NINJ1组成的环可以持续打开(图源:奇点网)
然而,当删除了NINJ1的α1和α2螺旋时,这个原本持续开放的圆环会在短短几十微秒内迅速关闭。
图7.失去α1和α2螺旋后,NINJ1环迅速闭合(图源:奇点网)
基于以上研究数据,Hiller团队认为,NINJ1的α1螺旋在细胞膜成孔过程中既能稳定NINJ1的丝,又能赋予可塑性,发挥着至关重要的作用。实验也表明,NINJ1的单丝和双丝(环)都具有破坏细胞膜的能力,双丝打开细胞膜的方式类似于拉链。
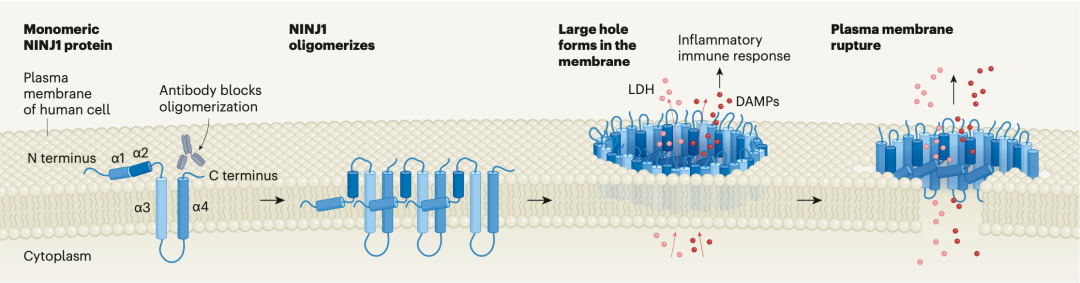
图8.机制示意图(图源:奇点网)
这两个研究表明,细胞程序性死亡相关的细胞膜裂解并不是被动的过程,而是一种由细胞自身调控的自主过程。当细胞接收到死亡信号后,NINJ1被激活,并形成丝状结构,导致细胞膜表面形成数百纳米到几微米的缺口,最终导致细胞膜裂解。
这些研究的意义在于,是否癌细胞的抗性死亡与NINJ1有关,是否可以利用NINJ1寻找新的方法杀死癌细胞;此外,细胞死亡也是引起神经退行性疾病、心血管等多种疾病的原因,因此寻找新的阻止细胞死亡、防止组织损伤的疗法也是很有意义的。
参考文献:
[1]Degen M, Santos JC, Pluhackova K, et al. Structural basis of NINJ1-mediated plasma membrane rupture in cell death. Nature. 2023;10.1038/s41586-023-05991-z. doi:10.1038/s41586-023-05991-z
[2]Kayagaki N, Stowe IB, Alegre K, et al. Inhibiting membrane rupture with NINJ1 antibodies limits tissue injury. Nature. 2023;10.1038/s41586-023-06191-5. doi:10.1038/s41586-023-06191-5
[3]Kayagaki N, Kornfeld OS, Lee BL, et al. NINJ1 mediates plasma membrane rupture during lytic cell death. Nature. 2021;591(7848):131-136. doi:10.1038/s41586-021-03218-7
文章来源于奇点网