2022年FDA批准的新药(附带全球已上市的45款基因治疗药物清单)
2022年,FDA的药品评价与研究中心(CDER)共批准了37款新药,包括22款新分子实体和15款生物制品。此外,生物制品评价和研究中心(CBER)还批准了2款疫苗、1款细胞疗法和4款基因疗法,以及1款微生物组疗法,共计45款。
与往年相比,今年FDA批准的新药数量有所下降,但创新含量极高,获批生物制品类型丰富,涉及单抗、双抗、ADC、TCR疗法、酶替代疗法等。
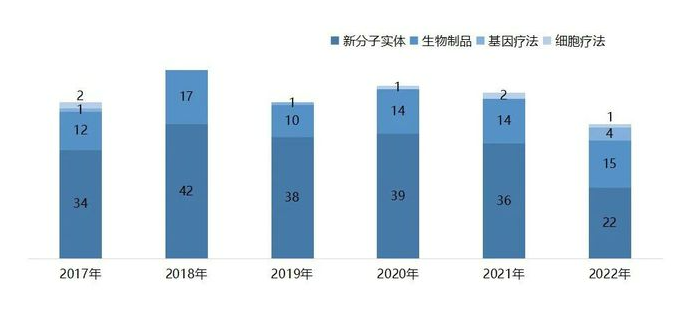
图1.历年FDA批准的新药数量
罕见病患者新药
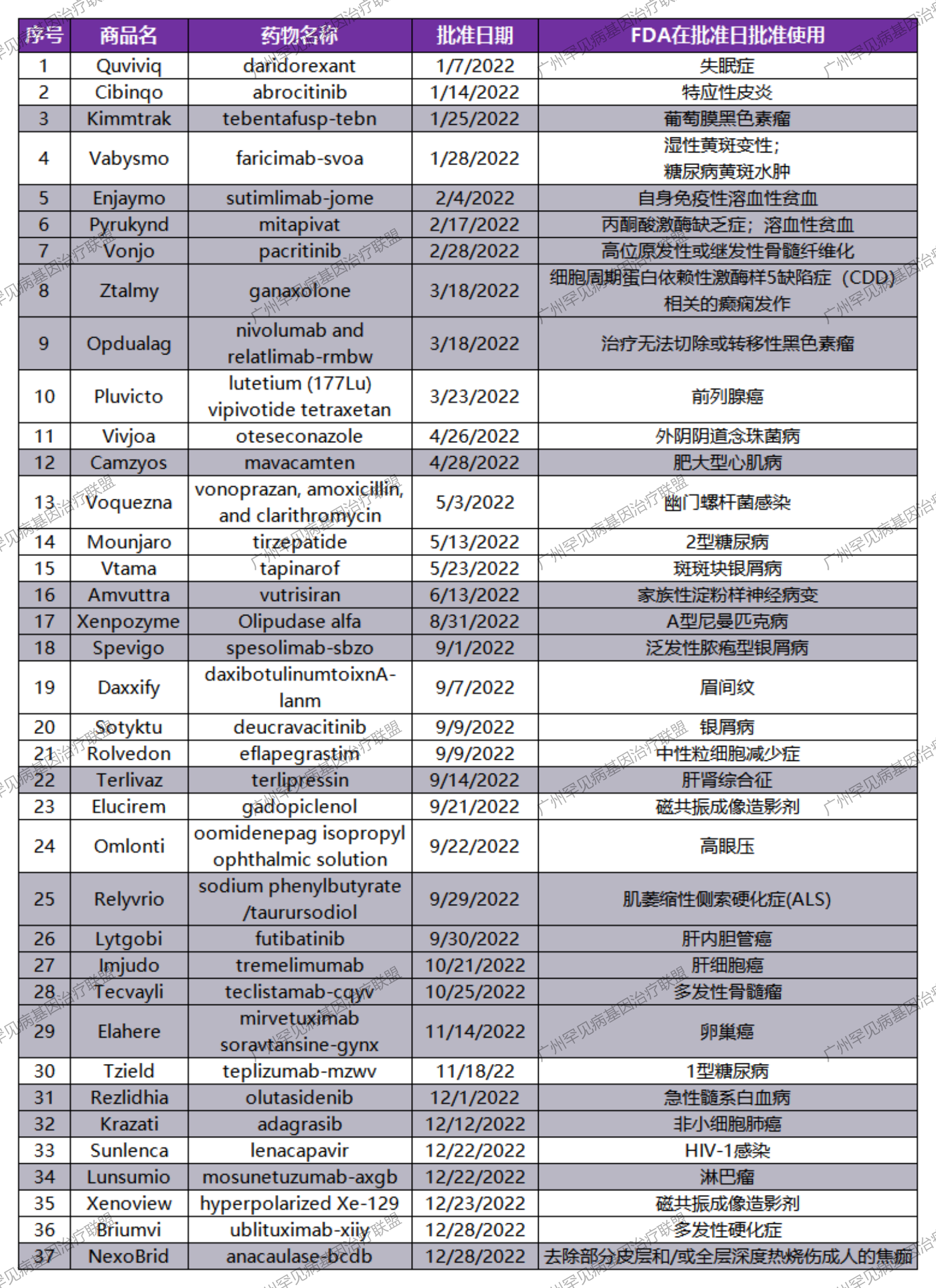
跟据联盟小编统计,下图是在2022年美国FDA一共批准的22个新分子实体和15个新生物制品,其中有20款被批准用于治疗罕见病或“孤儿病”(在美国影响不到20万人的疾病),表格中已标紫。
表1.2022年美国FDA一共批准的22个新分子实体和15个新生物制品
1.Amvuttra
注射剂治疗患有遗传性转甲状腺素蛋白介导的淀粉样变性的成年人的多发性神经病(全身多处神经损伤),这是一种导致器官和组织功能障碍的疾病。
2.Camzyos
用于治疗患有症状性纽约心脏协会(NYHA)II-III级梗阻性肥厚型心肌病(梗阻性HCM)的成人,以改善功能能力和症状。
3.Elahere
注射剂治疗对铂类疗法有抗性的复发性卵巢癌患者。
4.Enjaymo
注射剂以减少患有冷凝集素病(一种罕见的贫血症)的成人溶血(红细胞破坏)引起的红细胞输注。
5.Imjudo
注射剂与lmfinzi联合使用,治疗不可切除的肝细胞癌(最常见的肝癌类型)。
6.Kimmtrak
注射剂是转移性或不可切除的葡萄膜黑色素瘤的首个治疗药,葡萄膜黑色素瘤是一种发生在眼内葡萄膜的罕见癌症。
7.Krazati
用于治疗KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者,这些患者此前至少接受过一次全身治疗。
8.Lunsumio
注射剂治疗成人复发性或难治性滤泡性淋巴瘤(一种非霍奇金淋巴瘤)。Lunsumio通过加速审批计划获得批准。
9.Lytgobi
用于治疗携带FGFR2基因重排(包括基因融合)的局部晚期或转移性胆管癌患者,这些患者此前接受过一种或多种系统治疗。
10.NexoBrid
富含菠萝蛋白酶的蛋白水解酶浓缩物,是一种局部给药的生物制品,可在应用后四小时内酶促去除深度局部和全层热烧伤患者的无活性烧伤组织或焦痂,而不会伤害有活力的组织。
11.Opdualag
注射剂治疗12岁或以上患者的转移性或不可切除黑色素瘤。
12.Pyrukynd
片剂用于治疗丙酮酸激酶缺乏症(一种导致红细胞过早破坏的遗传性疾病)的成人的溶血性贫血(红细胞破坏速度快于生成速度的疾病)。
13.Relyvrio
用于治疗肌萎缩侧索硬化症(ALS)的口服溶液粉剂,ALS是一种影响脑和脊髓神经细胞的进行性神经退行性疾病。
14.Rezlidhia
用于治疗IDH1疑似突变的复发或难治性急性髓性白血病(AML)的成人患者。
15.Spevigo
注射剂治疗泛发性脓型银屑病(一种危及生命的皮肤病)的发作。Spevigo是首个获批治疗这种疾病的方法。
16.Tecvayli
注射剂用于治疗先前已接受过至少四种治疗的成人复发性和难治性多发性骨髓瘤。Tecyayli通过加速审批计划获得批准。
17.Terlivaz
注射剂以改善肝肾综合征成人患者的肾功能,肝肾综合征是晚期肝病患者肾功能受损的一种罕见形式。Terlivaz是首个获批治疗这种疾病的药物。
18.Vonjo
胶囊,用于治疗患有罕见骨髓疾病(称为中危或高危原发性或继发性骨髓纤维化)且血小板(凝血细胞)水平低于50,000/uL的成年人。Vonjo通过加速审批计划获得批准。
19.Xenpozymei
输液治疗酸性鞘磷脂酶缺乏症(A,B,A/B型Niemann-Pick病)的非中枢神经系统表现。这是对这种影响人体脂肪代谢能力并可能影响肺、肝和脾脏的遗传性疾病的首个治疗药。
20.Ztalmy
口服混悬剂,治疗与细胞周期蛋白依赖性激酶样5(CDKL5)缺乏症(CDD)相关的癫痫发作。
细胞基因治疗药物
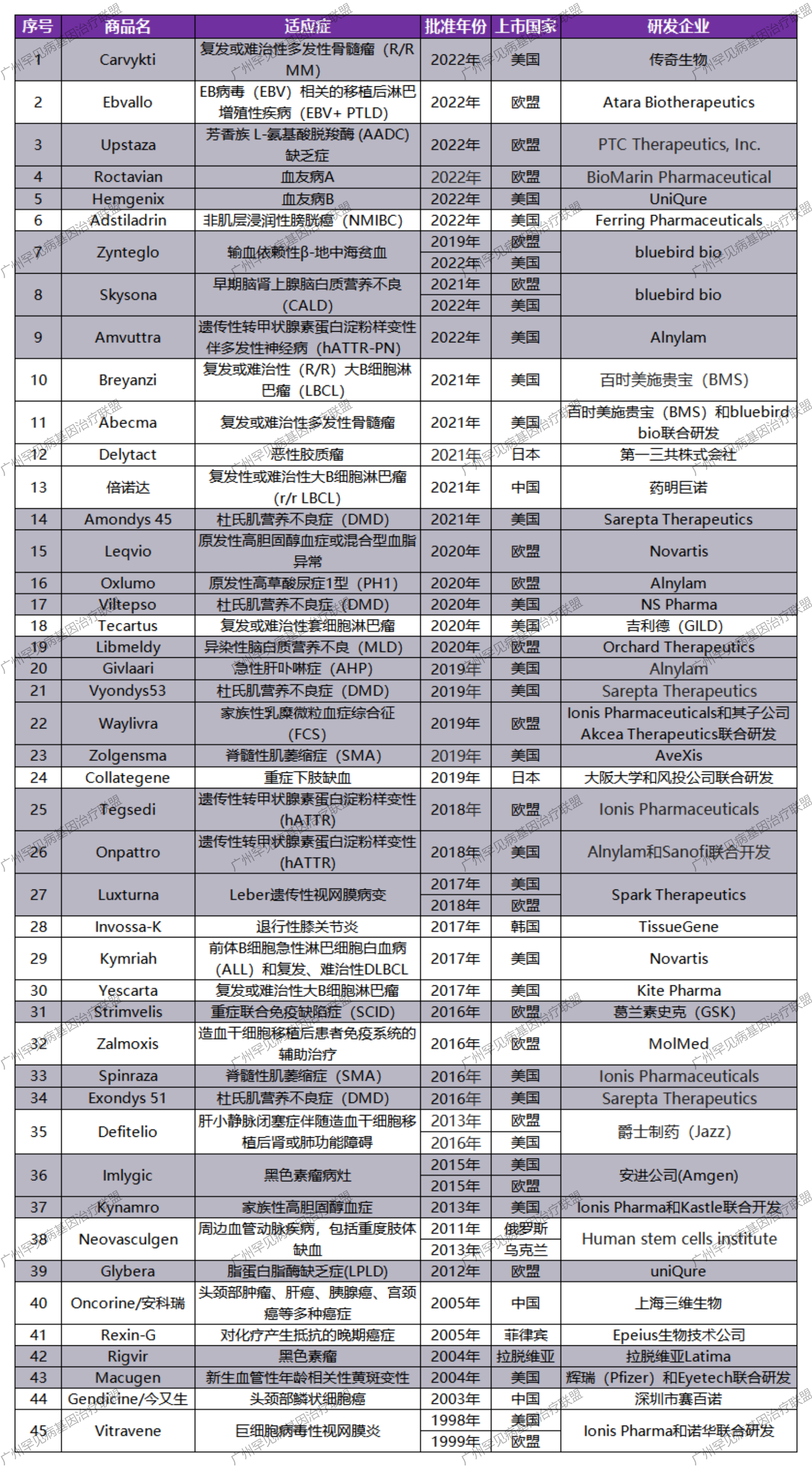
2022年FDA批准的基因疗法数量空前,高达4款,其中罕见病治疗药物有3款。由于罕见病人群狭窄,叠加成本高等因素,蓝鸟生物的Zynteglo在美国定价280万美元,Skysona定价300万美元,CSL Behring的Hemgenix定价更是达到了350万美元,成为全球最贵的药物。
除了基因疗法,FDA还批准了1款细胞疗法、1款微生物组疗法和2款疫苗,其中细胞疗法Carvykti是来自于中国本土企业传奇生物,也是首款获得FDA批准的国产CAR-T疗法。
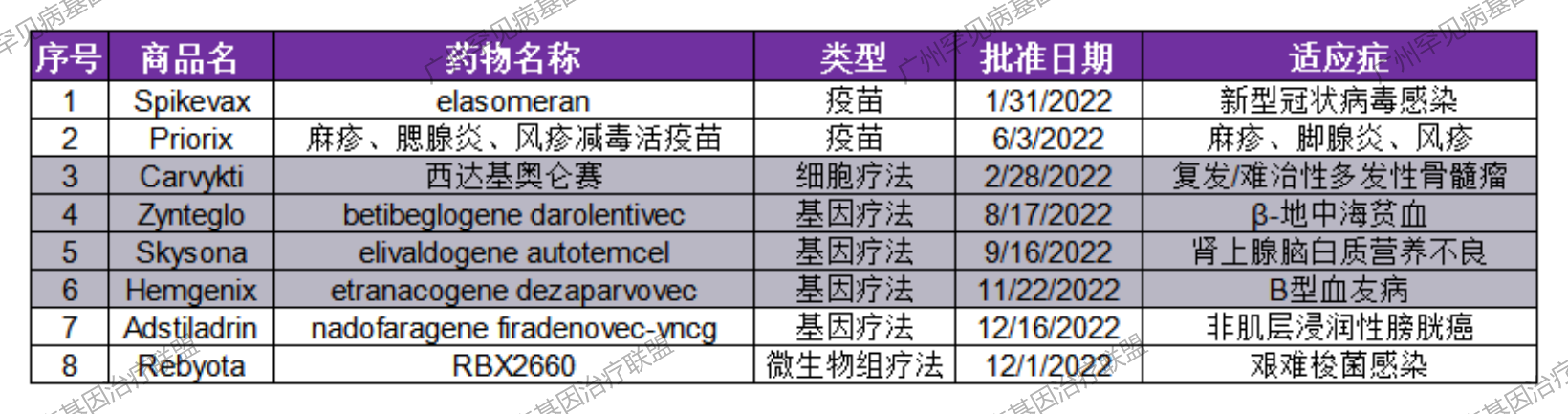
表2.2022年FDA批准的基因疗法
其中被批准用于治疗罕见病的细胞疗法和基因疗法药物有:
1.Carvykti
用于治疗复发/难治性多发性骨髓瘤,是一款靶向B细胞成熟抗原(BCMA)的嵌合抗原受体T细胞(CAR-T)疗法,使用CAR的转基因对患者自身的T细胞进行修饰,以识别和消除表达BCMA的细胞。Carvykti的CAR蛋白具有2种靶向BCMA单域抗体,对表达BCMA的细胞具有高亲和力,在与BCMA表达细胞结合后,CAR可促进T细胞活化、扩增,继而清除靶细胞。
2.Zynteglo
用于治疗β-地中海贫血,是一款一次性基因治疗药物,通过慢病毒载体将β-珠蛋白基因导入到患者自身的造血干细胞中,以生产正常的血红蛋白,恢复红细胞功能,从而显著降低患者的输血需求。在理想情况下,患者甚至不需要进行输血治疗。
3.Skysona
用于治疗肾上腺脑蛋白质营养不良,是蓝鸟生物第二款上市的基因治疗药物,利用Lenti-D慢病毒载体(LVV)进行体外转导,将ABCD1基因的功能拷贝添加到患者自身的造血干细胞(HSC)中。
4.Hemgenix
用于治疗B型血友病,是一款基于腺相关病毒5(AAV5)的基因治疗药物,通过静脉输注一次性给药。Hemgenix由携带凝血因子IX基因的AAV5病毒载体组成。该载体将因子IX的Padua基因变体(FIX Padua)携带到肝脏的靶细胞中,产生比正常因子IX活性高出5-8倍的因子IX蛋白,提高血液中因子IX水平,从而达到治疗目的。
细胞基因治疗技术有望成为新浪潮
参考资料
1. FAD:Novel Drug Approvals for 2022
2.https://mp.weixin.qq.com/s/EiZ5MCRFnfV1VLyaP63LDw
3.https://baijiahao.baidu.com/s?id=1754076337009713760&wfr=spider&for=pc
声明:本文收集归纳的信息,如有错漏,欢迎批评指正!