FDA重磅批准!Sephience上市为PKU患者点亮生命之光
罕见病苯丙酮尿病(PKU)迎来新药!美FDA批准Sephience上市
2025年7月28日,PTC Therapeutics公司宣布,美国食品药品监督管理局(FDA)已批准其口服药物Sephience®(sepiapterin)用于治疗1个月以上幼儿及成人苯丙酮尿症(PKU)患者的高苯丙氨酸血症(HPA)。这一批准标志着PKU治疗领域的重大进展,为全球患者提供了首个针对广泛年龄层的口服疗法选择。
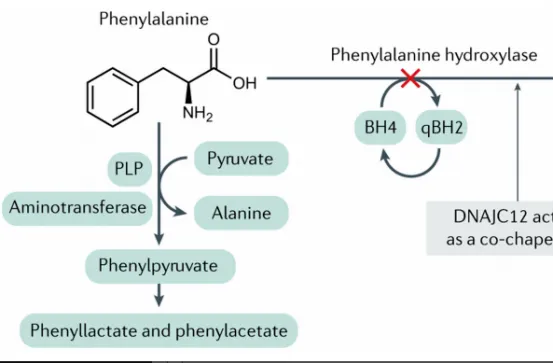
Sephience是一种口服BH4替代物,它通过模拟PAH辅因子(PAH基因突变是该病的致病原因)的功能,帮助恢复酶活性,从而大幅降低血液中苯丙氨酸的水平。临床试验显示,该药物可以使PKU患者的血液苯丙氨酸水平降低30%以上,且该治疗的不良反应轻微,大部分反应仅为轻度胃肠道不适,再加上药物是以口服片剂的形式服用,大大提高了PKU患儿的治疗方便性。
关于罕见病苯丙酮尿病(PKU)
苯丙酮尿病是一种罕见的遗传性代谢疾病,患者因为PAH基因突变,无法产生分解苯丙氨酸(Phe,一种存在于所有蛋白质中的必须氨基酸)的蛋白酶,从而导致氨基酸在体内积聚到有害水平,造成发育迟缓、癫痫发作、记忆丧失、甚至危及大脑,造成永久性智力障碍和不可逆的残疾!据统计,全球有58000人患有PKU。
尽管Sephience为PKU患者提供了新的治疗选择,但该药物仅能缓解患者的血液代谢问题、无法治本。好在研究人员并没有停止研发的脚步,在刚落幕的第28届美国基因与细胞治疗学会年会(ASGCT 2025)上,华毅乐健发布了公司自主研发的一款针对遗传性代谢病PKU的基因治疗候选药物GS1168,展现了中国创新力量在基因治疗领域的重要突破,有望实现“一次性治愈”!
华毅乐健验证了PKU患者中的突变型PAH会影响野生型PAH的功能,并基于此提出了GS1168的“双效一体治疗策略”,全新的治疗机制设计:使用优化的microRNA模块,有效沉默体内突变的PAH基因,避免功能干扰。同时通过AAV载体表达RNAi耐受、优化密码子的PAH蛋白,恢复正常功能。
这一设计创新型的将两种机制集成于一个AAV载体中,实现“打破干扰+重建功能”的双效治疗。
【声明】本文为转载文章,本平台仅作分享、传递信息,版权归原作者所有,如有侵权,请联系删除。