全球首创!光遗传学基因疗法正式提交BLA,开启治疗新纪元
日前,美国生物技术公司Nanoscope Therapeutics宣布,已经开始向FDA滚动提交其基于光遗传学的在研基因疗法MCO-010的生物制品许可申请(BLA),用于治疗色素性视网膜炎(RP)引起的严重视力丧失,无论其基因突变如何。
FDA已批准Nanoscope对其BLA进行滚动审查,首批模块已经提交,预计完整的BLA申请将于2026年完成。该申请有资格根据该项目的快速通道指定获得优先审查。
值得注意的是,这是全球进度最快的光遗传学基因治疗,已经提交BLA申请。同时,这是一个里程碑,标志着光遗传基因治疗取得重要进展。
MCO-010是一种环境光(Ambient light)激活的光遗传学基因疗法,利用AAV2载体将MCO基因递送到双极视网膜细胞中,使其表达多色视蛋白,同时利用光感受器死亡后剩余的视觉回路。该疗法适用于RP和Stargardt,不论潜在的基因突变如何。这种疗法一次性注入眼内,无需任何硬件设备。MCO1对环境光敏感,因此不需要将强光照射到眼睛中。
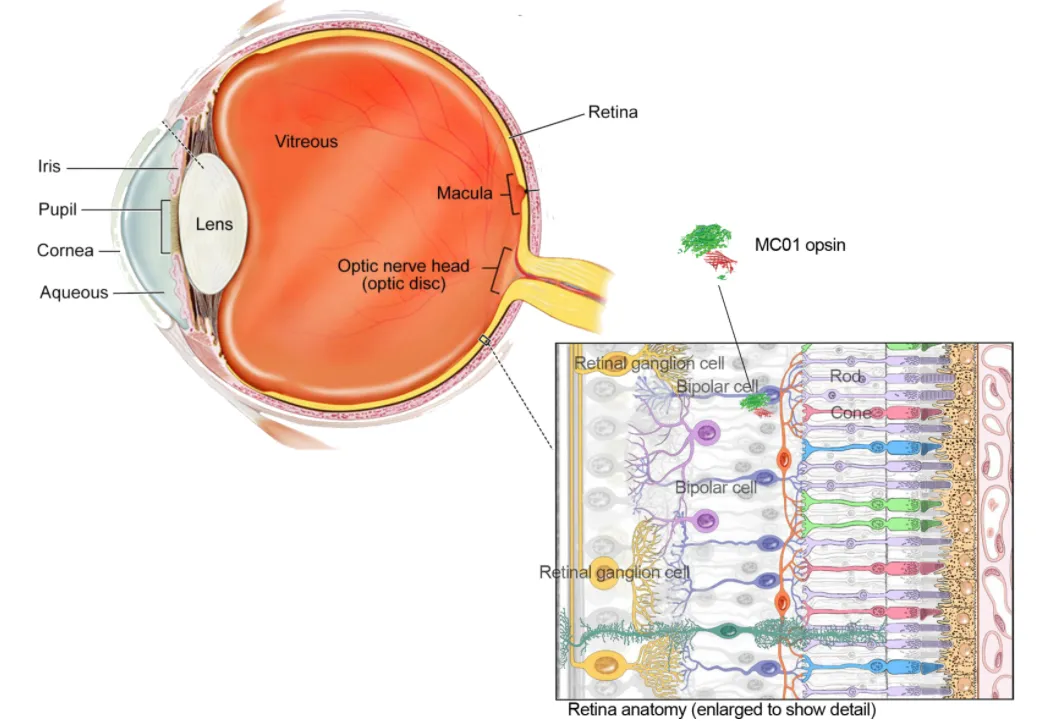
视网膜的结构及其双极细胞的位置、MCO-010基因药物表达MCO1视蛋白示意图
根据新闻稿,如果MCO-010获得批准,其将有可能成为RP的护理标准。因为RP可能的基因突变非常广泛,涉及100多个已知的基因以及1000多种不同的基因突变,而MCO-010的治疗与其基因突变无关,不需要进行基因检测,且为一次性治疗,也不需其他辅助治疗手段,具有良好的患者可及性。
光遗传学这一门学科自2002年正式产生雏形,到2006年正式成立学科,一度被认为是诺贝尔奖的潜在获奖者,吸引了不少研究者投入,越来越多的特异性光敏蛋白被发现。
事实上,光遗传学基因治疗的治疗范畴不仅只有眼科疾病,还涵盖了其他多种疾病领域,包括神经内科疾病、心脏内科疾病、代谢肥胖等。
另外,最近还有研究利用光遗传学进行药物筛选的应用。
来源:佰傲谷BioValley
【声明】本文为转载文章,本平台仅作分享、传递信息,版权归原作者所有,如有侵权,请联系删除。