异染性脑白质营养不良(MLD)有新药可用:FDA新批准Orchard Therapeutics一项细胞基因疗法
3月18日,Orchard Therapeutics宣布,美国FDA已批准其细胞基因疗法Libmeldy(OTL-200)用于治疗异染性脑白质营养不良(MLD),包括前症状性晚发婴儿型(PSLI)、前症状性早发青少年型(PSEJ)或早期症状性早发青少年型(ESEJ)儿科患者。

Libmeldy(又名OTL-200)使用慢病毒载体将编码芳基硫酸酯酶-A的ARSA转基因导入到患者自体CD34阳性造血干细胞和祖细胞中,该疗法已在欧盟获批用于治疗以ARSA基因双等位基因突变导致儿童ARSA酶活性降低为特征的MLD患者。Libmeldy是首个获批用于符合资格的早发性MLD患者的疗法。
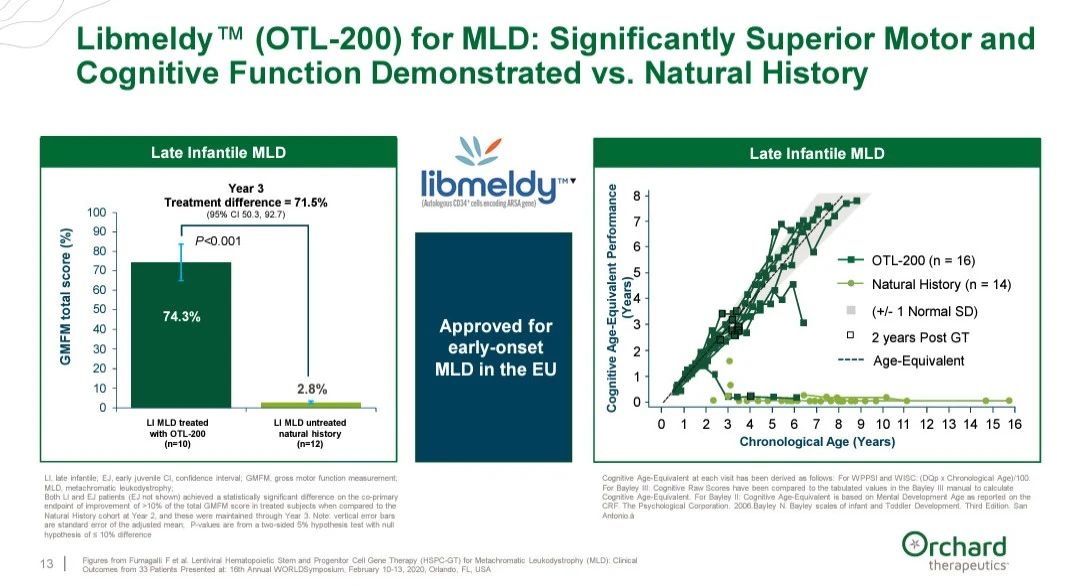
该BLA申请是基于39例早发性MLD儿科患者的数据,这些患者入组了两项前瞻性非随机临床研究(n=30)或在扩大使用框架下接受治疗(n=9),给予Libmeldy并与49例未接受治疗患者的自然史数据进行比较。在临床试验中,与疾病自然史相比,Libmeldy治疗可使大多数患者的运动功能和认知发育得以保留,随访时间长达12年(中位数6.76年)。Libmeldy成为美国唯一适合治疗早发异染性脑白质营养不良儿童的药物。
图1:Libmeldy试验结果,来源:Orchard Therapeutics 公开信息
MLD是一种罕见且危及生命的机体代谢系统遗传性疾病,根据现有文献估计发生率约为1/10万新生儿。MLD是由芳基硫酸酯酶-a(ARSA)基因突变引起的,导致硫酸盐在脑和身体其他区域蓄积,包括肝脏、胆囊、肾脏和/或脾脏。随着时间的推移,患者的神经系统会受损,导致其在运动、行为和认知上退化,并发生严重痉挛和癫痫发作等神经问题。MLD患者会逐渐丧失活动、说话、吞咽、进食和视物的能力。在婴儿晚期,发病后5年的死亡率估计为50%,10年的死亡率估计为44%。
关于Orchard Therapeutics
在Orchard Therapeutics,我们的愿景是结束基因疾病和其他严重疾病造成的破坏。我们的目标是通过发现、开发和商业化新的治疗方法,以发掘造血干细胞(HSC)基因治疗的治疗潜力。在这种方法中,患者自身的血液干细胞在体外进行基因改造,然后重新插入,目的是在单一治疗中纠正疾病的根本原因。
2018年,公司收购了GSK的罕见病基因疗法组合,该组合源于GSK与意大利米兰圣拉斐尔Telethon基因治疗研究所的开创性合作。如今,果园正在推进一项涵盖临床前、临床和商业阶段的HSC基因疗法,旨在应对严重疾病,这些疾病对患者、家庭和社会造成了巨大的负担,而目前的治疗方案有限或根本不存在。
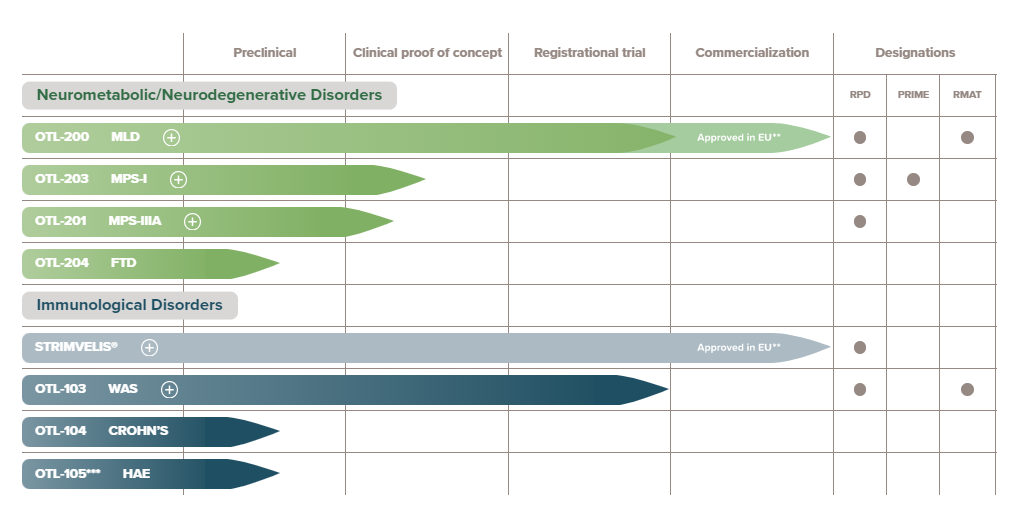
图2:Orchard Therapeutics研发管线,来源:Orchard Therapeutics 官网
来源:细胞基因疗法
【声明】本文为转载文章,本平台仅作分享、传递信息,版权归原作者所有,如有侵权,请联系删除。